Бэлтгэсэн : Дотрын эмгэг судлалын секторын ЭША Б.Тэгшжаргал
ХСВ нь Флавивиридае бүлгийн Хепасивирүсийн төрөлд хамаардаг, элгийг сонгомлоор гэмтээж, элэгний хурц болон архаг үрэвсэл үүсгэдэг вирүс юм. 1980-аад оны сүүлээр Майкл Хоугтоны ахласан эрдэмтэд өвчтний ийлдэсээс вирүсийн геномтой төстэй молекулыг илрүүлж, түүнтэй харилцан нэгдэх чадвар бүхий ДНХ лямбда фагийг ялган, гарган авч чадсан. Энэхүү судалгааны ажлын үр дүнд 9600 орчим нуклеотид бүхий маш том геномтой, дан РНХ утаслаг бүхий ХСВ нээхэд түлхэц болжээ. ХСВ нь жижигхэн, эерэг мушгиатай, 9.6 нм урттай РНХ агуулсан вирүс юм. Генийн дарааллыг нь 1989 онд анх удаа нээсэн1. Уг вирүс нь геномын хувьд нэлээд хувирамтгай, олон генотип, субгенотипээс бүрддэг2. ХСВ-ийн геномийн нуклеотидийн дараалал нь өөр хоорондоо 30% орчим ялгаатай долоон генотипд (1-7) хуваагддаг3. Harvey J.Alter, Michael Hougthon, Charles M.Rice нар ХСВ-ийн нээлтээрээ 2020 онд Нобелийн анагаах ухааны салбарт шагнал хүртсэн.
ХСВ тархалтыг anti-HCV-д үндэслэн тогтооход дэлхийн хүн амын 1% нь ХСВ халдвартай бөгөөд ойролцоогоор 71 сая хүн ХСВ-ийн халдвартай амьдарч байна. Үүнээс жил тутам 350 мянган хүн ХСВ-ийн хүндрэл болох элэгний цирроз, элэгний анхдагч өмөнгөөр нас барж байна. 2015 оны байдлаар нэг удаагийн бус зүү тариур болон ариутгаагүй эмнэлгийн багаж хэрэгслээс халдвар авч, жил бүр 1.75 сая хүн шинээр ХСВ-ийн халдвар авч байна4. ХСВ халдварласан ихэнх хүмүүс халдвар авснаа мэддэггүй бөгөөд оношлогдсон хүмүүсийн олонх нь ХСВ эсрэг эмчилгээнд хамрагдаж чадахгүй байна5. ХСВ–ийн архаг халдвартай хүмүүсийн гуравны нэг нь элэгний цирроз, элэгний анхдагч өмөн өвчнөөр өвчилдөг6.
ХСВ-ийн халдвар дэлхий дээр харилцан адилгүй тархсан байна. ХСВ-ийн тархалт нь Төв болон Зүүн ази, Хойд Африк, Ойрх дорнодод хамгийн өндөр байна. Харин Хойд Америк, Баруун Европ, Австралид бага тархалттай байна7 (Зураг). ХСВ-ийн халдварын тархалт нь бага болон дунд орлоготой орнуудад эрүүл мэндийн ялгаатай байдалтай нягт холбоотой байдаг. ХСВ-ийн халдвар ихэвчлэн зүү тариурын аюулгүй байдлыг сайн хангаагүй болон бөөрний гемодиализ хийлгэх, цус цусан бүтээгдэхүүнийг хяналтгүйгээр юүлэх зэрэг ажилбараар дамждаг8. ХСВ нь эхээс урагт халдварлах магадлал 4-8% байдаг бол эх ХСВ болон ХДХВ-ийн давхар халдвартай тохиолдолд халдварлах магадлал 17-25% байдаг9.
ХСВ-ийн генотип болон субтипүүд нь бүс нутгийн газарзүйн байршил, халдварлах зам, тархалтын хэмжээ зэргээс хамаарч харилцан адилгүй тархсан байдаг10. ХСВ-ийн 1 генотип дэлхийд өргөн тархсан (40-80%) бөгөөд генотип 1а, 1b АНУ-д, 1b Европ, Турк, Япон, Тайван ба Австралид зонхилон тархсан байна11. 2-р зургаас харахад манай орны хувьд ХСВ-ийн халдварын тархалт өндөр оронд хамаарч, 1b генотип нь ХСВ халдвартай нийт хүн амын 98.8% -ийг эзэлж байна.
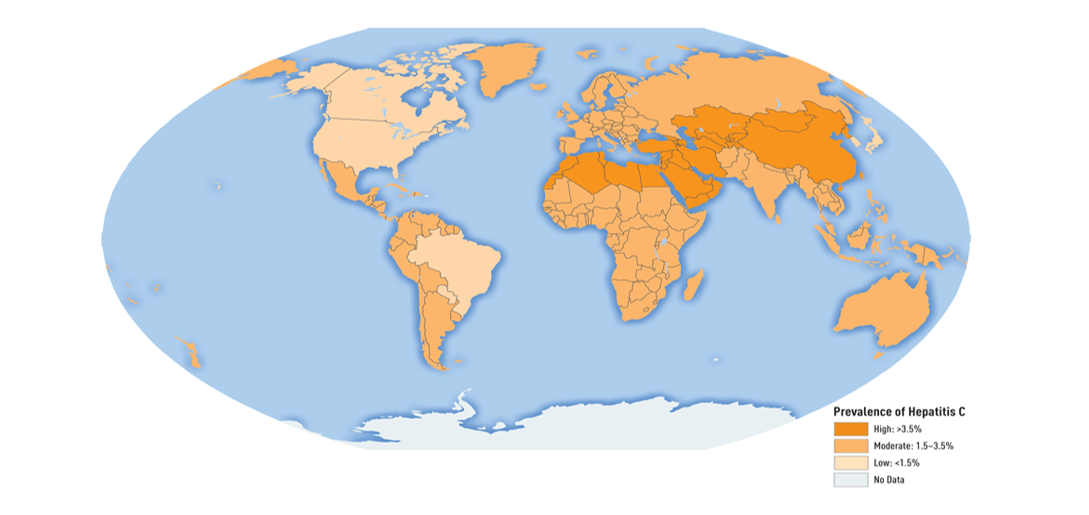
Зураг. ХСВ-ийн халдварын тархалт (CDC 2016)
Монгол улсад 1b генотип давамгайлж байгаа нь сүүлийн үед шинээр хийгдэж буй ХСВ эсрэг эмчилгээ болох шууд үйчилгээтэй антивирүс агентууд (DAAs) маш өндөр үр дүнтэй байхад нөлөөлж байна12. Монгол улсын насанд хүрэгчдийн дунд хийсэн судалгаагаар ХСВ-ийн халдварын тархалт 8.5% байна13. Манай орны хүн амын дунд эмнэлэгт олон удаа хэвтэх, мэс ажилбар хийлгэх, аборт хийлгэх мөн бэртэл гэмтэл авах зэрэг ХВВ, ХСВ-ийн халдварт өртөх олон халгаат хүчин зүйл оршиж байна. Ялангуяа төрөх, цус алдах, цус сэлбүүлэх, кесар хагалгаа хийлгэх нь эрсдэл ихтэй хүчин зүйл юм. Мөн тэдэнтэй ажилладаг эмч, эмнэлэгийн ажилтнууд нэгэн адил эрсдэл ихтэй хүн амын бүлэг юм. Хүн амын энэ бүлэгт хийсэн зарим судалгаанд тэдэнд тохиолдож буй архаг хепатит болон циррозын 20.8%, 27% нь ХСВ-ийн шалтгаантай байжээ. ХСВ-ийн халдвартай өвчтөнүүдийн 15-30%-д 20 жилийн дотор элэгний хатуурал үүсэх эрсдэлтэй. Элэгний хатууралтай хүмүүст элэгний хорт хавдар үүсэх эрсдэл жил тутамд 2-4%-иар ихэсдэг14. ХСВ-ийн халдвар ихэнхдээ эмнэлзүйн шинж тэмдэг бага байх ба цөөн тохиолдолд амь насанд аюултай хүнд хэлбэрээр илэрнэ. Халдвар авсан хүмүүсийн 15-40% эхний 6 сарын дотор өөрөө аяндаа эдгэрч, 55-85% нь эмчлүүлэхгүй бол насан туршдаа ХСВ-ийг архаг халдвар тээгч болдог15. ХСВ ийн халдвараас урьдчилан сэргийлэх вакцин байхгүй. ХСВ ээс урьдчилан сэргийлэхийн тулд халдварт өртөх эрсдэлээс урьдчилан сэргийлэх хэрэгтэй. Халдварт өртөх эрдэлд тариур, цус цусан бүтээгдэхүүн сэлбэх үед, нэг удаагийн бус багажаар мэс ажилбар , шүдний эмчилгээ, үзлэг, шивээс хийлгэх арьсаа цоолуулах зэрэг нь ордог. ХСВ-ийн халдварыг эмчлэх нилээд хэдэн эм байгаа бөгөөд сүүлд үйлдвэрлэгдсэн вирүсийн эсрэг шууд үйлчилгээтэй эмүүд нь халдварыг 90 гаруй хувийн үр дүнтэй эмчилж байна. ХСВ-ийн халдварын эмчилгээнд одоогоор батлагдсан эмчилгээ нь стандарт Интерферон альфа (ИФН-α), Пэг-интерферон (Пэг-ИФН), рибавирин (РБВ), протеазыг саатуулагчид (ПС) болох боцепревир, телапревир, симепревир ба NS5B, нуклеотид полимеразыг саатуулагч буюу софосбувир зэрэг багтдаг16.
Ном зүй
- Houghton M. The long and winding road leading to the identification of the hepatitis C virus. Journal of hepatology. Nov 2009;51(5):939-948.
- Simmonds P. Reconstructing the origins of human hepatitis viruses. Philosophical transactions of the Royal Society of London. Series B, Biological sciences. Jul 29 2001;356(1411):1013-1026.
- Nakano T, Lau GM, Lau GM, Sugiyama M, Mizokami M. An updated analysis of hepatitis C virus genotypes and subtypes based on the complete coding region. Liver international : official journal of the International Association for the Study of the Liver. Feb 2012;32(2):339-345.
- Polaris Observatory HCVC. Global prevalence and genotype distribution of hepatitis C virus infection in 2015: a modelling study. The lancet. Gastroenterology & hepatology. Mar 2017;2(3):161-176.
- Lemoine M, Nayagam S, Thursz M. Viral hepatitis in resource-limited countries and access to antiviral therapies: current and future challenges. Future virology. Apr 2013;8(4):371-380.
- Ly KN, Xing J, Klevens RM, Jiles RB, Ward JW, Holmberg SD. The increasing burden of mortality from viral hepatitis in the United States between 1999 and 2007. Annals of internal medicine. Feb 21 2012;156(4):271-278.
- Mohd Hanafiah K, Groeger J, Flaxman AD, Wiersma ST. Global epidemiology of hepatitis C virus infection: new estimates of age-specific antibody to HCV seroprevalence. Hepatology. Apr 2013;57(4):1333-1342.
- Candotti D, Sarkodie F, Allain JP. Residual risk of transfusion in Ghana. British journal of haematology. Apr 2001;113(1):37-39.
- Mast EE, Hwang LY, Seto DS, et al. Risk factors for perinatal transmission of hepatitis C virus (HCV) and the natural history of HCV infection acquired in infancy. The Journal of infectious diseases. Dec 1 2005;192(11):1880-1889.
- Smith DB, Pathirana S, Davidson F, et al. The origin of hepatitis C virus genotypes. The Journal of general virology. Feb 1997;78 ( Pt 2):321-328.
- Strader DB, Wright T, Thomas DL, Seeff LB, American Association for the Study of Liver D. Diagnosis, management, and treatment of hepatitis C. Hepatology. Apr 2004;39(4):1147-1171.
- Kurbanov F, Tanaka Y, Elkady A, Oyunsuren T, Mizokami M. Tracing hepatitis C and Delta viruses to estimate their contribution in HCC rates in Mongolia. Journal of viral hepatitis. Sep 2007;14(9):667-674.
- Davaalkham D. APASL-STC. Ulaanbaatar, Mongolia2017.
- El-Serag HB, Rudolph KL. Hepatocellular carcinoma: epidemiology and molecular carcinogenesis. Gastroenterology. 2007;132(7):2557-76
- Thomson EC, Fleming VM, Main J, et al. Predicting spontaneous clearance of acute hepatitis C virus in a large cohort of HIV-1-infected men. Gut. 2011;60(6):837-45
- Sulkowski MS, Rodriguez-Torres M, Lalezari JP, et al. All oral therapy with sofosbuvir plus rivavirin for the treatment of HCV genotype 1, 2 and 3 infection in patients co-infected HIV. 64th Annual meeting of American Association for the Study of Liver Disease (AASLD 2013) Washington, DC, USA:1-5 November.



Recent Comments